上海大学高兴华团队《Adv. Healthc. Mater.》:基于中空微纤维组装的内分泌胰腺芯片,用于糖替代品评估
发布日期:2023-12-29
浏览量:636次
近年来,非传染性疾病(NCD),如II型糖尿病、心血管疾病和高血压等已经成为了全球的主要死亡原因。在这其中,过量摄入高热量糖与肥胖和许多非传染性疾病风险高度相关。已有研究表明,减少高热量糖的过量摄入可以降低患龋齿、肥胖、糖尿病、高血压和癌症的风险。因此,随着人们对低糖、低热量健康饮食的需求不断增加,人工甜味剂在食品工业中作为糖替代品的需求越来越高。相应的,这些糖替代品对人体的影响评估就显得极为必要。
近期,上海大学材料基因组工程研究院高兴华团队提出了一种用于糖替代品食品添加剂安全性评价的微流控芯片。该工作开发了一种基于微纤维组装的内分泌胰腺芯片,将基于微流控纺丝技术制备的模拟血管与3D胰岛培养芯片相结合,可以用于评估葡萄糖以及各种糖替代品对胰岛细胞活力以及胰岛素、胰高血糖素分泌的影响,进而对其进行食品安全性评价。相关研究以“Hollow Microfiber Assembly-Based Endocrine Pancreas-on-a-Chip for Sugar Substitute Evaluation”为题发表在《Advanced Healthcare Materials》期刊上。
如图1所示,通过微流控纺丝技术,研究人员使用甲基丙烯酰化明胶(GelMA)与海藻酸钙(CaA)制备了可负载细胞的中空复合微纤维,用于模拟血管组织并用于物质运输。同时,研究人员使用Matrigel作为细胞外基质(ECM)材料,构建了三维胰岛组织,与复合微纤维一同组装到芯片中即可构建得到内分泌胰腺芯片。
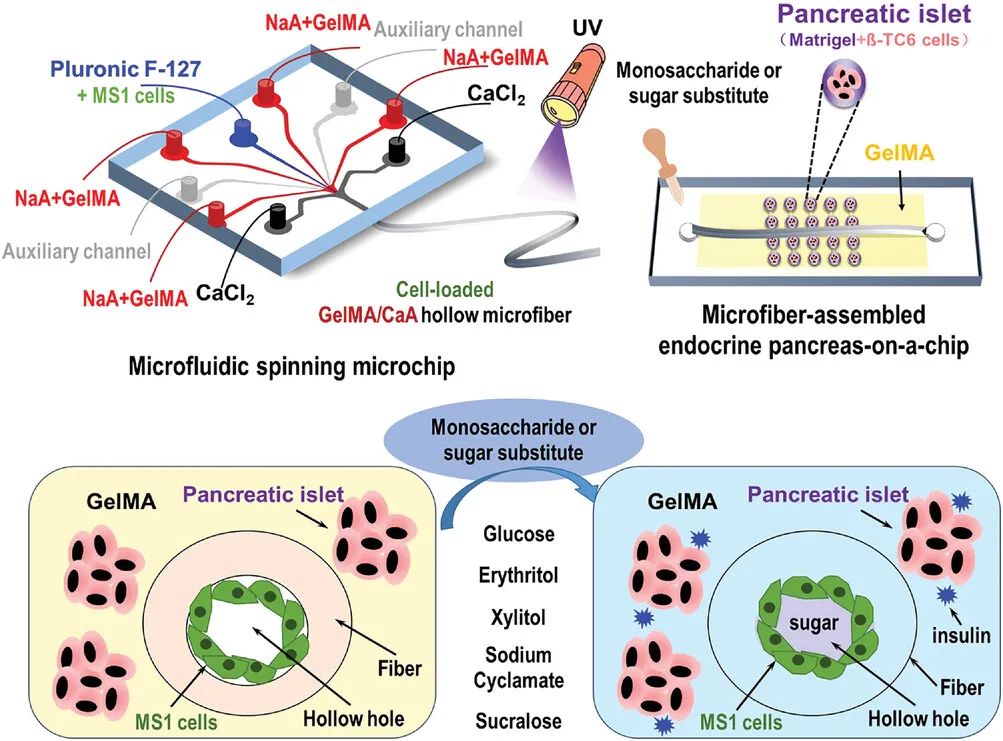
图1 利用微流控纺丝技术构建内分泌胰腺芯片
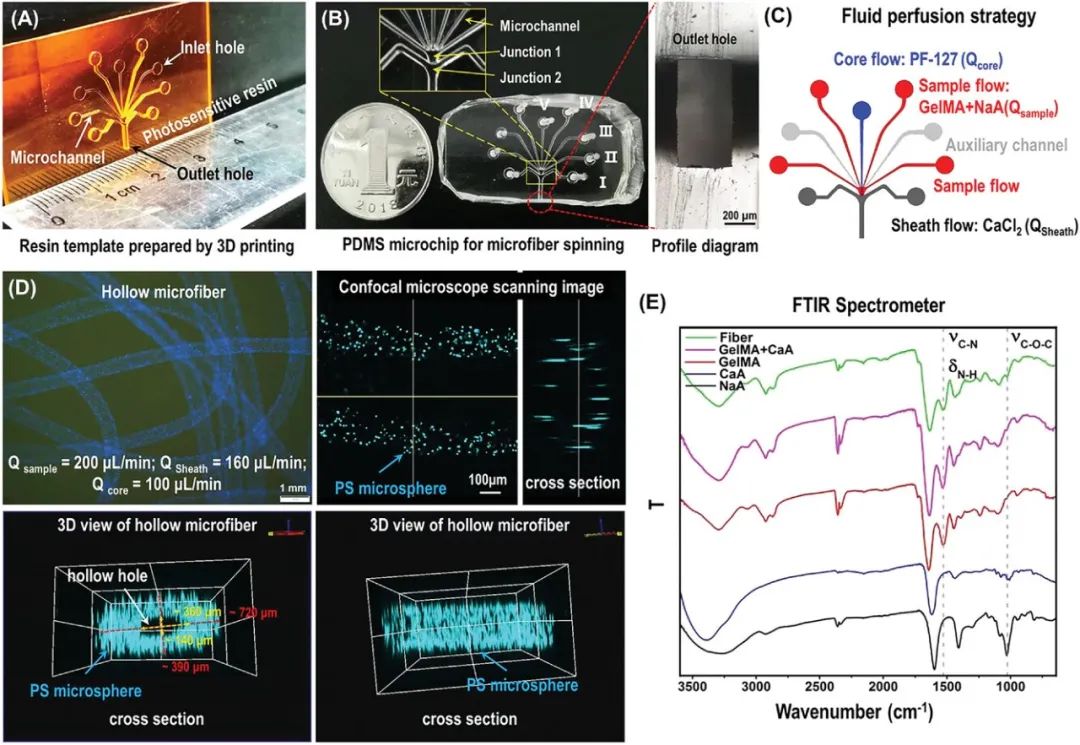
图2展示了微流控纺丝技术制备GelMA/CaA中空微纤维的方法与表征。GelMA是一种具有良好生物相容性的血管化构建常用材料,将其与CaA进行共混使用,可以得到具有双交联网络的优质血管支架材料。该团队使用摩方精密nanoArch®S140(精度:10μm)制备了具有不同高度流道的芯片模板,并使用PDMS成型得到微纤维制备芯片。通过在芯片的不同流道中通入不同的组分或辅助流体,材料中的海藻酸盐(NaA)与钙离子(Ca²⁺)可以发生瞬时离子交联对微纤维进行快速定形,再通过紫外曝光使GelMA二次交联,最终得到尺寸均匀、结构完整的复合微纤维。
目前,血管模型构建中的细胞加载通常存在两种方法,一是将细胞加载到中心流道中,使内皮细胞粘附在流道侧壁上进行生长;另一种则是将细胞加载到外侧管状凝胶中,使凝胶作为上皮细胞的支架进行三维培养。如图3所示,研究人员同时采用了两种方法接种小鼠胰岛内皮细胞(MS1),最终确定加载到中心流道中的方法能带来明显更佳的效果,细胞在中空微纤维中可以形成管腔结构,且表现出一定的血管化内皮特性。
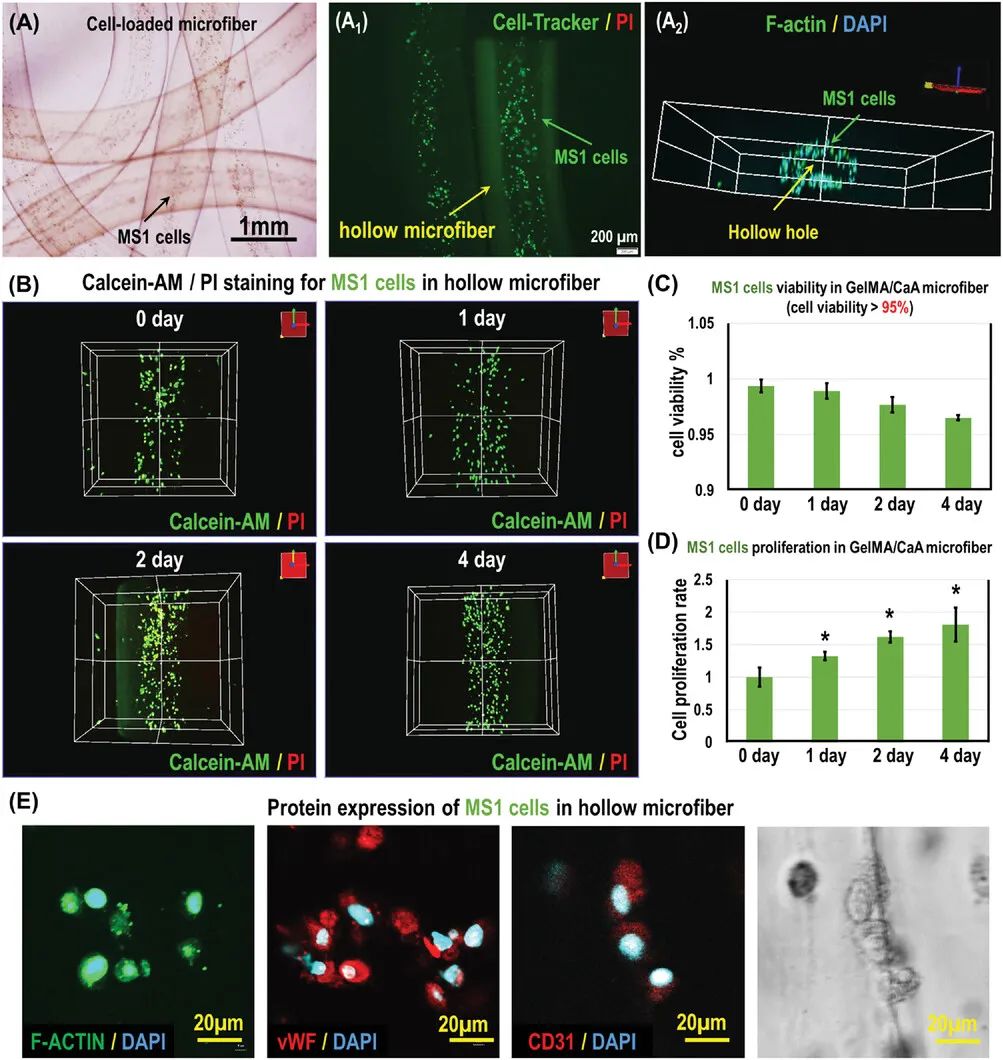
图3 GelMA/CaA复合中空微纤维的细胞加载与培养
通过上述方法构建得到模拟血管组织后,研究人员将其与三维胰岛培养组织结合,得到内分泌胰腺芯片。如图4所示,小鼠胰岛瘤胰岛β细胞(β-TC6)在芯片上Matrigel中成簇生长,细胞内与编码、产生胰岛素等相关的mRNA均能正常表达。
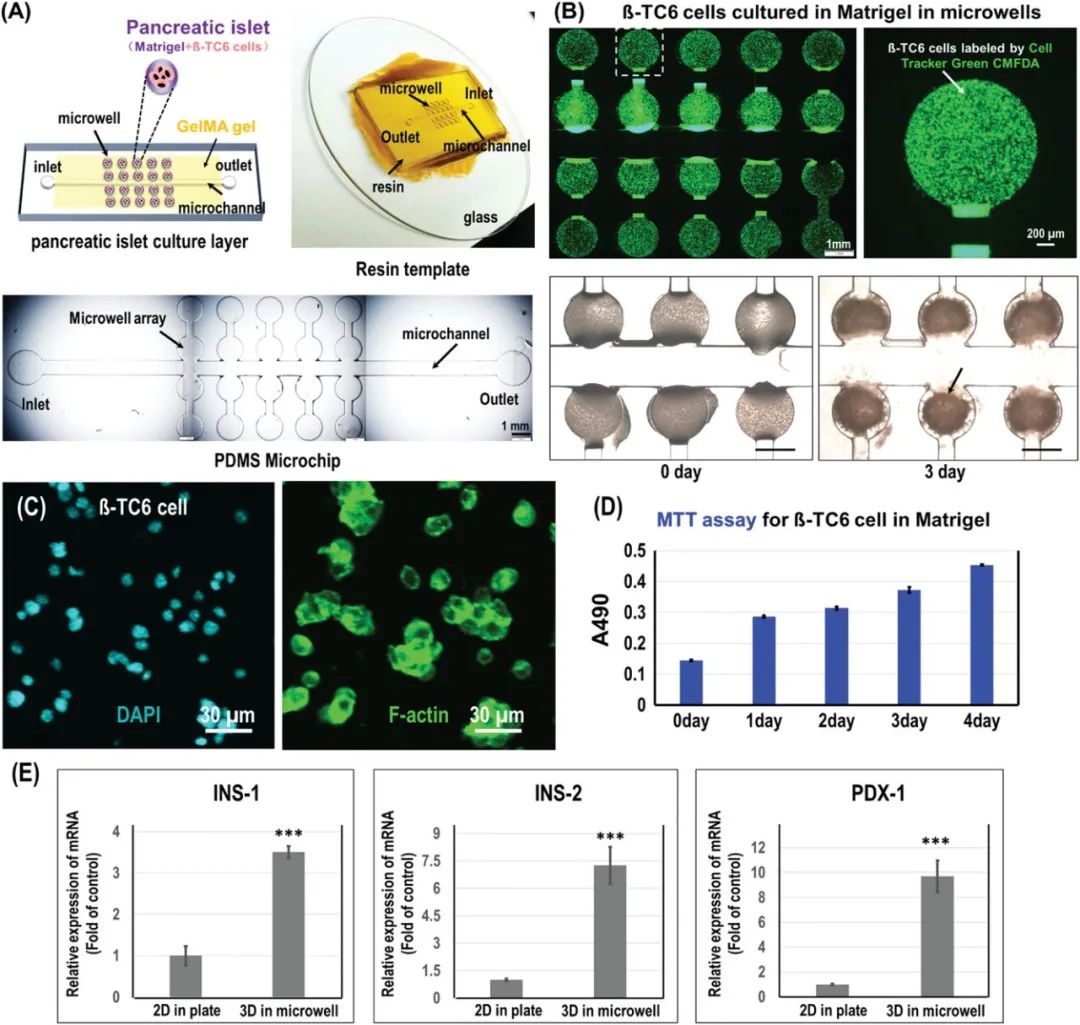
图4 胰岛组织的三维培养及表征
内分泌胰腺芯片在嵌入微纤维模拟血管以及三维胰岛培养组织后,研究人员使用GelMA水凝胶对其进行覆盖。模拟血管在芯片培养一定时间后表现出了良好的可灌注性与渗透性,如图5所示。研究人员通过模拟血管向芯片中通入不同浓度的葡萄糖溶液,可以实现对胰岛培养组织的持续动态刺激,高葡萄糖浓度溶液可以显著提高胰岛培养组织中胰岛素的分泌量,且这种变化相较于静态培养组更加明显,更加接近生理状态,可以更准确地评估糖代谢。
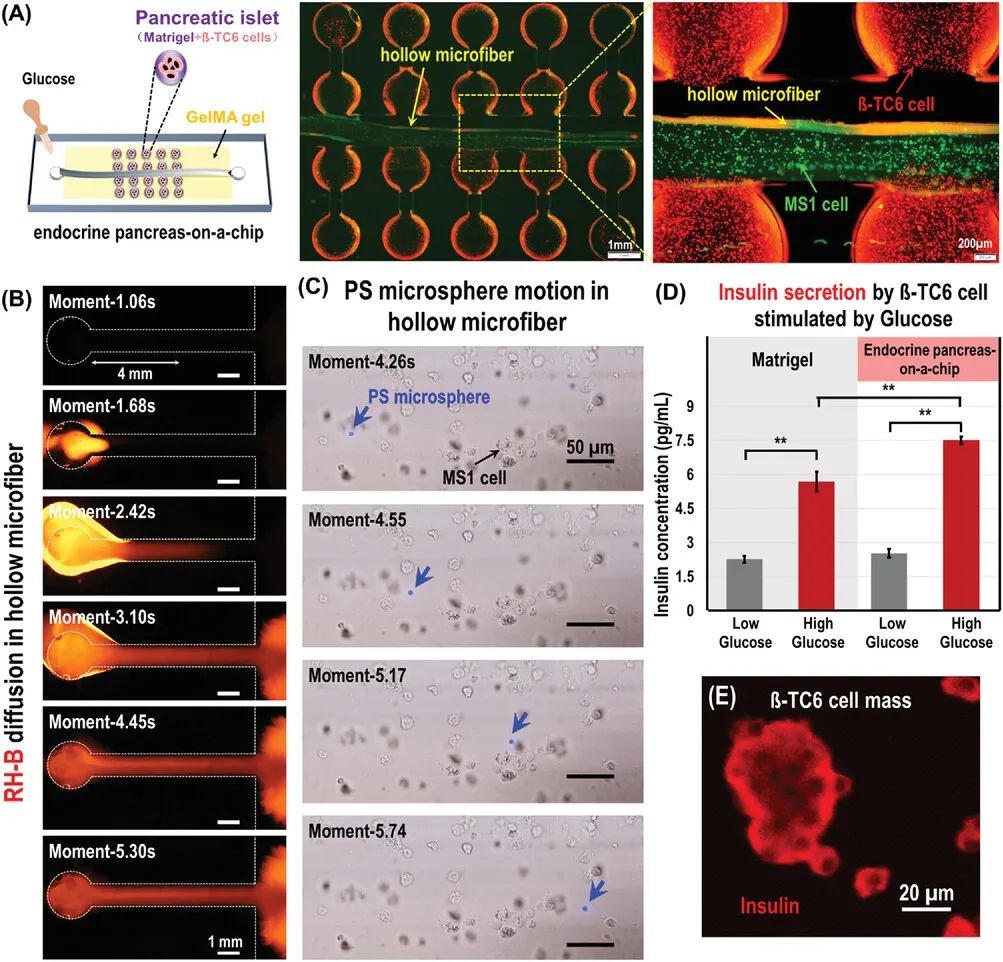
图5 内分泌胰腺芯片的构建与表征
基于该种内分泌胰腺芯片,研究人员对四种常见的糖替代品:赤藓糖醇、木糖醇、糖精钠和三氯蔗糖进行了安全性评价,如图6所示。评价结果显示,四种糖替代品均不会刺激胰岛产生更多的胰岛素,而与胰岛素相拮抗的胰高血糖素则出现分泌量显著上升,这些结果足以说明上述糖替代品不会导致血糖水平的上升。
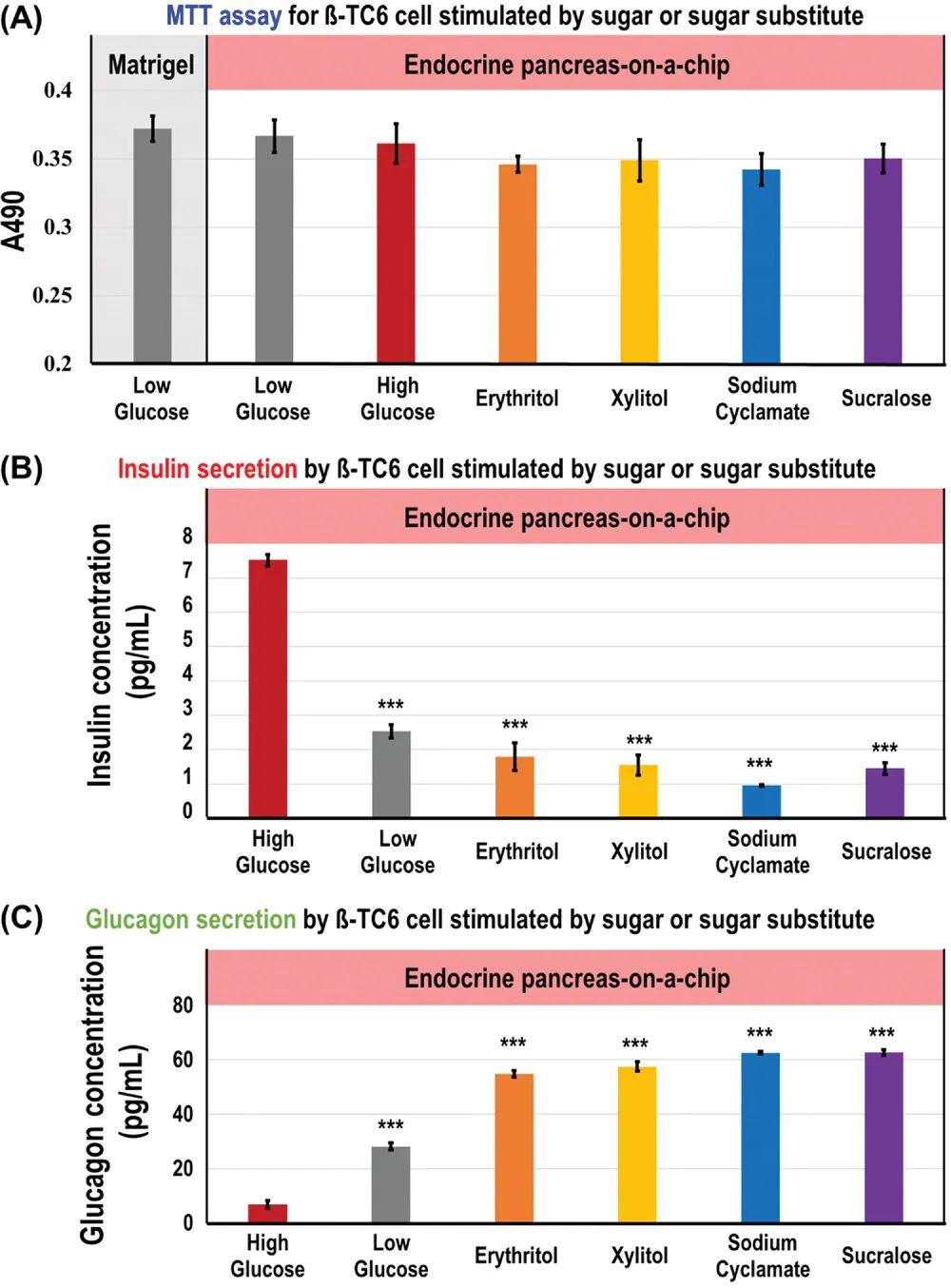
图6 基于内分泌胰腺芯片的糖替代品安全性评价
综上所述,该研究开发了一种新型的、基于中空微纤维模拟血管的内分泌胰腺芯片,可用于评价糖替代品对胰岛细胞的活力以及胰岛素、胰高血糖素分泌量的影响,为各类食品添加剂的安全性评价提供新的平台。该芯片还在胰岛疾病体外生理模型构建、药物评价、胰岛体外仿生设计等方面具有着潜在的应用价值。
论文链接:https://doi.org/10.1002/adhm.202302104